Stratégie de contrôle de la contamination et amélioration continue des API stériles lyophilisées
Préface
L'industrie pharmaceutique est une industrie de soutien à la santé humaine. Avec l'intensification du vieillissement de la population mondiale et l'épidémie de Covid-19 d'événement d'urgence de sécurité publique, la demande humaine de médicaments ne cesse de croître. L'API est la base des produits pharmaceutiques. L'augmentation de la demande de produits pharmaceutiques a entraîné une augmentation de la demande d'API, ce qui a ensuite entraîné une augmentation de la demande de main-d'œuvre. Cependant, le vieillissement de la société maintient la diminution de notre population en âge de travailler. Par conséquent, la mise à niveau de la capacité de production pour la fabrication d'API est impérative, ce qui peut être réalisé en améliorant l'automatisation pour réduire la demande de travailleurs manuels.
Les API stériles sont des API préparées par des processus aseptiques. La préparation d'API aseptiques « non stérilisés de manière terminale » nécessite non seulement de la main-d'œuvre, mais également des personnes qualifiées, formées et qualifiées, et soumises à une gestion. L'annexe 1 « Production de médicaments stériles » de l'UE-BPF souligne que les sociétés pharmaceutiques doivent développer et améliorer en permanence leurs stratégies de contrôle de la pollution. Les êtres humains sont la plus grande source de pollution dans les processus aseptiques, pour lesquels Truking a établi des stratégies de contrôle de la pollution et sa propre capacité d'améliorations techniques continues pour les API stériles lyophilisés, grâce à une pratique à long terme dans la production d'API stériles lyophilisés .
|
Source
|
Risque de Pollution
|
|
Usine
|
Des flux de personnel et de matériel déraisonnables entraînent des confusions et de la pollution
|
|
Système de Filtration d’Air
|
Pollution d'humidité ou de poussière causée par le nombre de changements d'air, l'alimentation en air, le retour d'air et l'échappement d'air.
|
|
Equipement de Procédé
|
Le processus et l'équipement ne correspondent pas, ce qui entraîne une diminution de la capacité de production et de la qualité
|
|
Personnel
|
Des facteurs tels que le niveau de santé, le professionnalisme, les habitudes de caractère et les compétences professionnelles affectent l'ensemble du processus de production de drogue
|
Conception de la zone centrale de fabrication d'API aseptiques lyophilisés
Conception de Système
Basées sur le principe Qbd, les bonnes pratiques de production découlent d'une bonne conception du système. Le mode de fabrication ouvert des API lyophilisés traditionnels est un facteur important qui entraîne de nombreux risques de pollution. Par conséquent, changer le système ouvert en système fermé est la première solution pour contrôler la pollution.
|
Type de Fabrication
|
Application de ce guide en étapes (montré en gris) utilisée pour ce type de fabrication
|
|
Fabrication Chimique
|
Production des API
Matières Premières
|
Introduction de l’API Matière Première dans le procédé
|
Production d’intermédiaires
|
Isolation et Purification
|
Procédé Physique et Emballage
|
|
API dérivés de sources animales
|
Collection de fluide organique ou tissu
|
Coupage, mélange et/ou procédé initial
|
Introduction de l’API Matière Première dans le procédé
|
Isolation et Purification
|
Procédé Physique et Emballage
|
|
API extraits de sources végétales
|
Collection des plantes
|
Coupage et extraction initiale
|
Introduction de l’API Matière Première dans le procédé
|
Isolation et Purification
|
Procédé Physique et Emballage
|
|
Extraits d’herbe utilisés comme API
|
Collection des plantes
|
Coupage et extraction initiale
|
|
Extraction supplémentaire
|
Procédé Physique et Emballage
|
|
API consistant en herbes broyées et poudrées
|
Collection des plantes et/ou culture et récolte
|
Coupage / Broyage
|
|
|
Procédé Physique et Emballage
|
|
Biotechnologie : Fermentation/Culture Cellulaire
|
Etablissement de banque de cellules maitresses et banque de cellules de travail
|
Maintenance de la =banque de Cellules de travail
|
Culture cellulaire et/ou fermentation
|
Isolation et purification
|
Procédé Physique et Emballage
|
|
Fermentation Classique pour production d’API
|
Etablissement de banque de cellules
|
Maintenance de la =banque de Cellules de travail
|
Introduction des cellules dans la fermentation
|
Isolation et purification
|
Procédé Physique et Emballage
|
Figure 1 : Application de ce guide à la fabrication d'API (ICH Q7a)
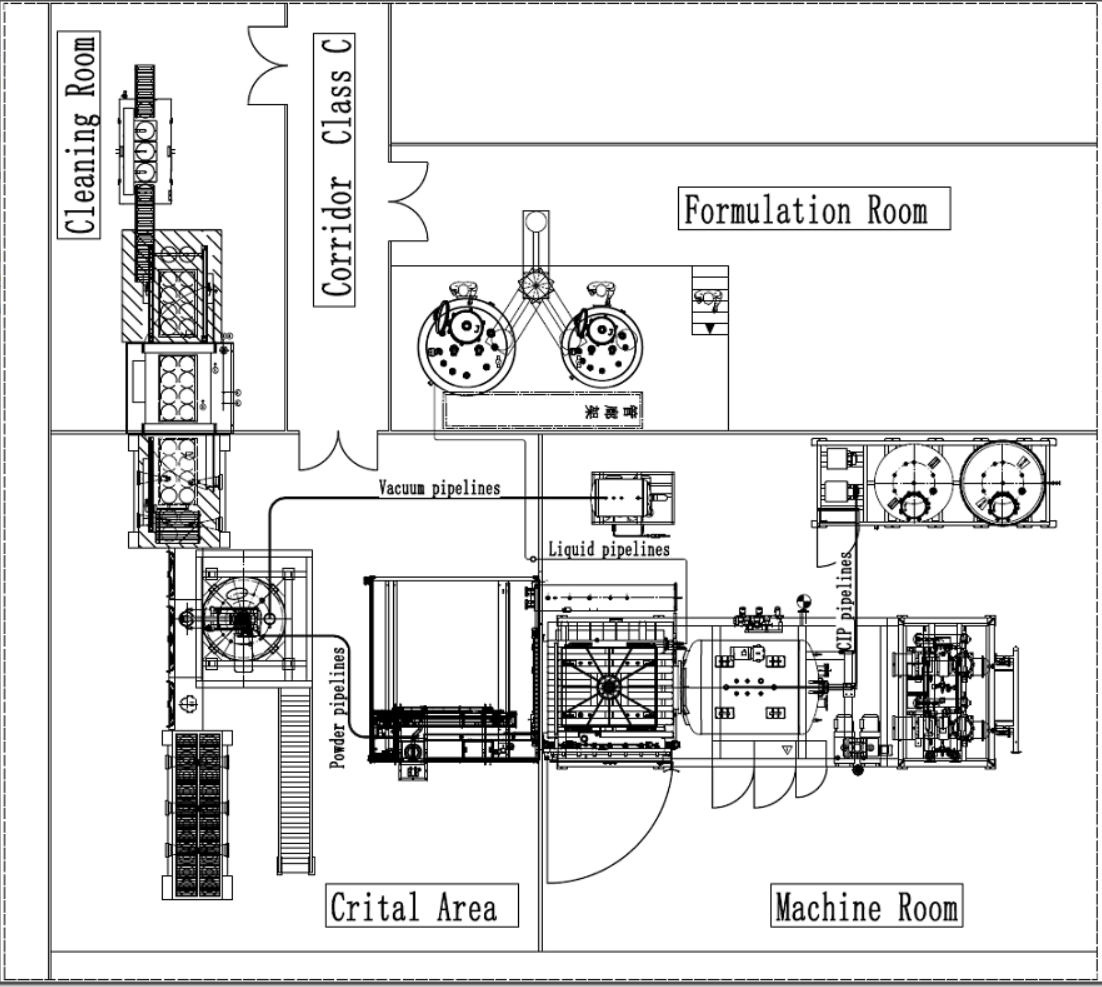
Un atelier API stérile lyophilisé complet comprend principalement (mais sans s'y limiter) des cuves de préparation, des filtres, des dispositifs de chargement, un lyophilisateur sous vide, des dispositifs de déchargement, une station CIP, un pulvérisateur, un mélangeur, une remplisseuse, une capsuleuse et un isolateur, etc.
Disposition conceptuelle d'un atelier API aseptique lyophilisé basé sur un isolateur
Lyophilisateur
le lyophilisateur a des bords pliés autour de l'étagère, qui a pour fonction de contenir directement le médicament liquide, réduisant ainsi les outils utilisés dans la zone aseptique ;
L'étagère est équipée d'un orifice de décharge. Lorsque toutes les étagères descendent, l'orifice de décharge s'ouvre automatiquement pour drainer l'eau de nettoyage à l'intérieur de l'étagère et s'assurer que les étagères sont bien nettoyées
L'étagère peut monter et descendre et a les fonctions de remplissage de produit à hauteur égale et de déchargement de produit à hauteur égale;
Le dispositif de chargement est intégré dans le lyophilisateur, et la fonction de chargement télescopique de chaque étagère peut être réalisée par le mouvement de l'étagère ;
Le lyophilisateur est équipé d'une porte à fente automatique et le déchargement du produit s'effectue en ouvrant la porte à fente pour réduire la zone d'exposition à la poussière ;
Le dispositif de déchargement est entièrement automatique, ce qui réduit les opérations humaines ;
Déchargement du produit à hauteur égale, petit déplacement dans le sens vertical de l'équipement, avec une faible hauteur de l'appareil ; vitesse du vent uniforme du système d'écoulement unidirectionnel de toute la surface de travail de déchargement et dans la plage contrôlable de la valeur guide, facile à vérifier, et aucune base scientifique supplémentaire n'est requise ;
Un dessin d'ensemble de lyophilisateur avec une porte de fente de déchargement
Isolateur
L'isolateur est hautement intégré à la porte de déchargement, au dispositif de déchargement et au dispositif de remplissage aseptique du lyophilisateur, et la surface de travail centrale de l'opération de déchargement est placée sous protection à flux unidirectionnel dans l'isolateur ;
L'isolateur est équipé d'un système de climatisation indépendant pour contrôler le volume d'air, la température et l'humidité de la zone centrale aseptique afin d'éliminer complètement l'influence des installations de l'usine sur la zone centrale aseptique ;
Le système de barrière de l'isolateur élimine complètement les interventions manuelles involontaires, garantissant que le comportement des opérateurs en cours de processus est contrôlable et que les opérateurs sont complètement isolés ;
l'isolateur a son propre système de nettoyage et le système de désinfection assure la propreté et la stérilité de l'équipement.
Un équipement intégré de lyophilisateur, isolateur et dispositif de déchargement
Stratégie de contrôle des risques
|
source
|
Stratégie de contrôle des risques
|
|
Usine
|
Le processus et l'équipement sont hautement intégrés et la zone centrale aseptique est réalisée grâce à des isolateurs et à l'automatisation
|
|
Système de filtration d’air
|
Système de climatisation séparé pour zone centrale aseptique
|
|
Equipement de procédé
|
L'adéquation du processus et de l'équipement peut réduire le risque de processus de fabrication de médicaments
|
|
personnel
|
Isoler les opérateurs de la zone centrale stérile.
|
Résumé
Une bonne conception est la condition préalable pour garantir la mise en œuvre du processus aseptique et la qualité du produit. Truking continuera d'améliorer le niveau intelligent de fabrication d'API aseptiques lyophilisés grâce à une pratique continue d'ingénierie pharmaceutique.
Document de Référence
Bonnes pratiques de fabrication des médicaments (révisées en 2010)
Directives pharmaceutiques BPF : préparation stérile
Directives GMP pharmaceutiques : API
EU GMP Annexe 1:Fabrication de produits stériles
 400-9988-900
400-9988-900




 Téléchargement de fichiers
Téléchargement de fichiers




